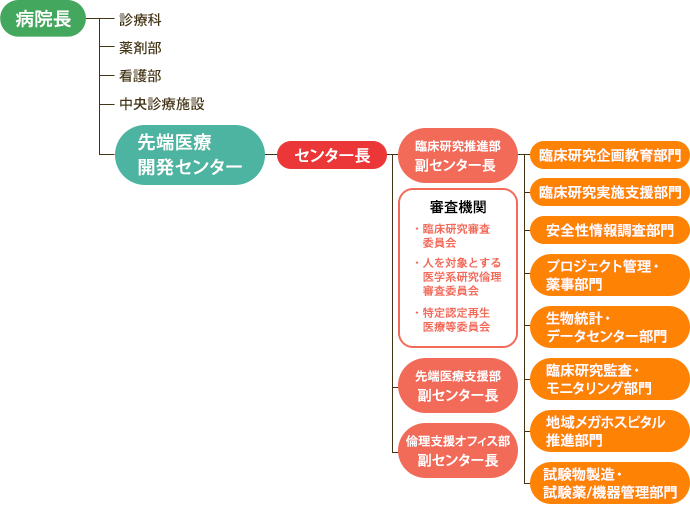
組織
先端医療開発センター臨床研究推進部は新薬の開発治験のみでなく、製造販売後臨床試験、製造販売後調査、検査用試薬、治療用手技、医療機器の臨床研究も扱うものとする。
企業治験支援部門
- 治験事務局
- CRC支援
- 治験薬管理
- 製販後調査支援
- 臨床検査業務支援
臨床研究支援部門
- 研究事務局
- 研究コンサルテーション
- CRC支援・データ入力支援
- プロジェクトマネジメント
- データマネジメント
- モニタリング
- 生物統計
- データサイエンス推進室
治験・臨床研究管理部門
- 治験、臨床研究、再生医療等の審査委員会事務局業務
・臨床研究審査委員会(IRB・CRB)
・人を対象とする医学系研究倫理審査委員会
・特定認定再生医療等委員会
研究開発支援部門
臨床研究教育・広報部門
- 研究者教育
- 学生・大学院教育
- 臨床研究支援人材教育・養成
- 社会への広報活動
- 臨床研究における患者市民参画(PPI)の推進
- 地域臨床研究ネットワーク構築および各施設との連携