※1 新規物質の探索・創製
薬になりそうな新しい物質を探したり、作り出したりすること。
※2 物理的化学的研究
新規物質の構造や物理的・化学的な性状などを調べること。
※3 薬効薬理研究
どのような効果があるか、どのようなメカニズムで効果を現すのかなどを調べること。
※4 薬物動態研究
どのように、体内に吸収され、臓器などに分布し、代謝されて排泄されるかなどを調べること。
※5 一般薬理研究
どのような部位にどんな作用を及ぼすかなど、薬効薬理作用以外の安全性に関する作用を調べること。
※6 一般毒性研究
投与期間を短・中・長期などに分けて、毒性(安全性)を広く調べること。
※6 特殊毒性研究
発がん性や胎児への影響がないかなど、特別な毒性(安全性)を調べること。
※7 臨床第I相試験(臨床薬理試験)
少数の健康成人などについて、主に安全性や薬物動態などを調べる試験。
※8 臨床第II相試験(探索的試験)
比較的少数の患者さんについて、有効性と安全性などを調べる試験。
※9 臨床第III相試験(検証的試験)
多数の患者さんについて、標準的な「くすり」などと比較して有効性と安全性を確認する試験。
※10 製造販売後調査
製造販売後に多くの患者さんに使用されたときの安全性や有効性などの情報を集め、それを分析・
評価して医療関係者などに伝えること。
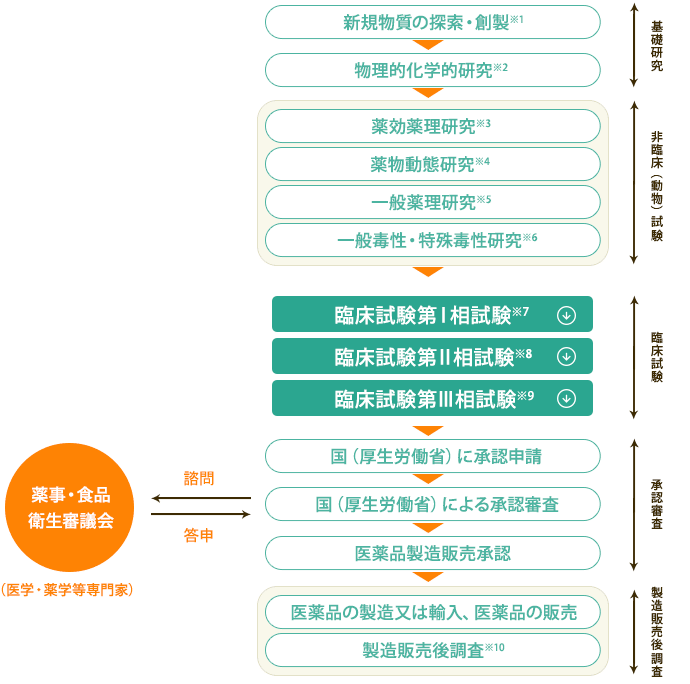
治験は、通常以下の3つのステップ(相)を踏んで進められます。

まず、少人数の健康成人において、ごく少量から少しずつ「くすりの候補」の投与量を増やしていき、安全性はどうかについて調べます。また、血液や尿などの中に存在する「くすりの候補」の量を測ることにより、どのくらいの速さで体内に吸収され、どのくらいの時間でどのように体外に排泄されるのかも調べます。
体に現れた変化が「くすりの候補」の副作用かどうかを見きわめるため、プラセボ(有効成分が入っていない、見た目や味などの点で「くすりの候補」と区別がつかないもの)を同時に使って比較することもあります。
「くすりの候補」の種類によっては、効果があると予想される患者さんから治験を始める方が適当なことがあり、この場合には効き目についても予備的に調べることができるのが普通です。
この最初のステップを『第I相試験』(臨床薬理試験)と言います。

次は、「くすりの候補」が効果を示すと予想される比較的少人数の患者さんについて、病気の程度によってどのような効き目を発揮するのか(有効性)、副作用はどの程度か(安全性)、またどのような使い方(投与量・間隔・期間など)をしたらよいか、といったことを調べます。効き目や使い方を調べるのに当たっては、通常いくつかの投与量を用いて比較検討しますが、その際にプラセボを加えるのが一般的です。また現在使われている標準的な「くすり」がある場合には、それと比較することもあります。
このステップを『第II相試験』(探索的試験)と言います。

最後に、多数の患者さんについて、第II相試験の結果から得られた「くすりの候補」の有効性、安全性、使い方を最終的に確認します。 確認の方法は、現在使われている標準的な「くすり」がある場合にはそれとの比較、標準的な「くすり」がないときにはプラセボとの比較が中心になります。 これとは別に、長期間使用したときの有効性や安全性がどうかを調べることもあります。
この最後のステップを『第III相試験』(検証的試験)といいます。
ここまでで、「くすりの候補」とプラセボや標準的な「くすり」との比較、あるいは「くすりの候補」の投与量の間の比較があることを述べました。科学の原則は比較することにあると言われていますように、治験を科学的に行ううえで、こうした比較試験は大変重要です。
しかし、比較試験はかたよりがなく公平に行われなければ意味がありません。そのため、一方には重症の患者さんが多く、他方には軽症の患者さんが多い、試験の時期が違う、あるいは先入観が入る、といったことのないようにする必要があります。
そこで、治験に参加される患者さん等をどの処置に割り付けるかは、くじを引くような方法で決め(「無作為化割り付け」と呼ばれます)、そのうえ、治験を行う医師や患者さん等のいずれにも、どの処置が割り付けられているのかが分からないようにする方法(「二重盲検法」と呼ばれます)が採られることも少なくありません。そしてどの処置も同時期に試験を行います。
以上の3つのステップを終了したところで、「くすり」を開発している製薬企業がそれらのデータを全てまとめて国(厚生労働省)に「くすり」として認めてもらうよう申請します。
国(厚生労働省)の厳正な審査をパスし、承認されることによって初めて、「くすりの候補」が「くすり」となるのです。